北航蔡軍課題組:基于小球藻細胞的磁性復合多聚體微機器人用于高效靶向給藥
發布日期:2022-04-14
瀏覽量:899次
微納機器人在低雷諾數流體中可將能量轉化為有效運動,因此在生物醫學領域具有巨大的應用前景。近年來,磁性微納機器人作為一種有發展前景的靶向給藥平臺而受到了特別的關注。科研工作者設計了不同的磁性微納機器人用于高效遞送抗癌藥物至靶向腫瘤部位并取得了較好的效果。研究發現,作為體內給藥的平臺或載體,一方面,微納機器人的生物相容性是至關重要;另一方面,微納機器人的重構對于其在復雜變化環境中高度靈活地完成給藥具有重要意義。然而,目前來說,微納機器人的研究在同時滿足這兩方面的要求上仍具有一定的挑戰性。
天然生物模板具有良好的生物相容性和精致結構的固有優勢,有望為磁性微納機器人的制備提供新的機遇。小球藻是一種具有良好的生物相容性和生物降解性的單細胞微藻。它們具有均勻的球狀結構,直徑約為3-5μm。這些特性使它們具有作為理想天然生物材料用于生物醫學領域的優越性。然而,由于扇貝定理的限制,在低雷諾數流體中采用動態磁場有效地驅動具有簡單對稱球體形狀的單一微球是不可行的,這限制了微藻細胞在微機器人領域的應用潛力。
近日,北京航空航天大學蔡軍課題組制備了一種基于小球藻細胞的磁性復合多聚體微機器人,實現了高效的靶向給藥。研究者將小球藻(Chlorella,Ch.)細胞作為一種生物模板,依次進行Fe3O4沉積、抗癌藥物阿霉素(DOX)裝載,實現磁性復合微機器人單元的制備。利用磁偶極作用,微機器人單元通過誘導自組裝作用重構成鏈狀的復合多聚體微機器人(BMMs),如微小的二聚體、三聚體等。基于面投影微立體光刻(PμSL)微納3D打印技術設計了啞鈴形的微流控通道,用于進行BMMs的體外靶向給藥試驗(圖1)。
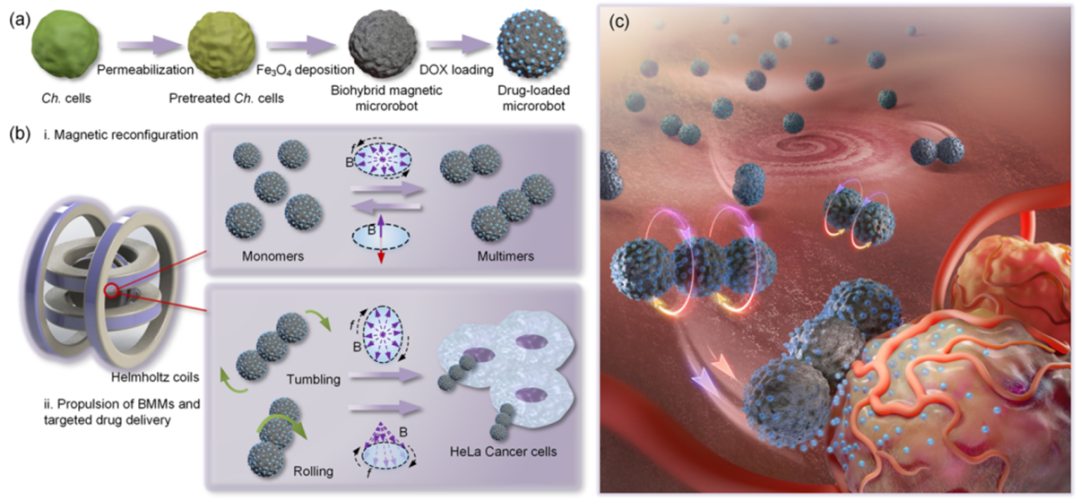
圖1,BMMs的制備和靶向給藥示意圖。
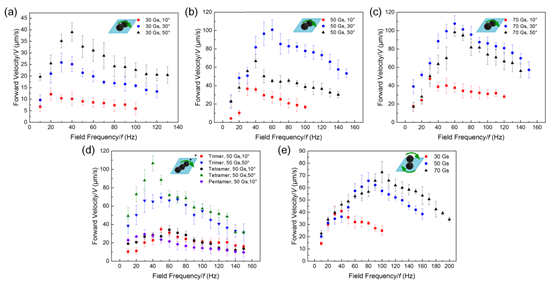
圖2,自組裝BMMs的驅動性能。
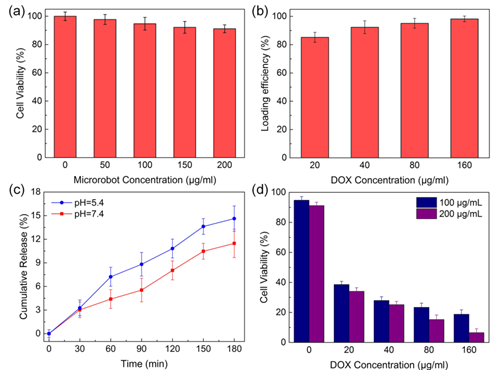
圖3,BMMs的生物相容性和化療性能。
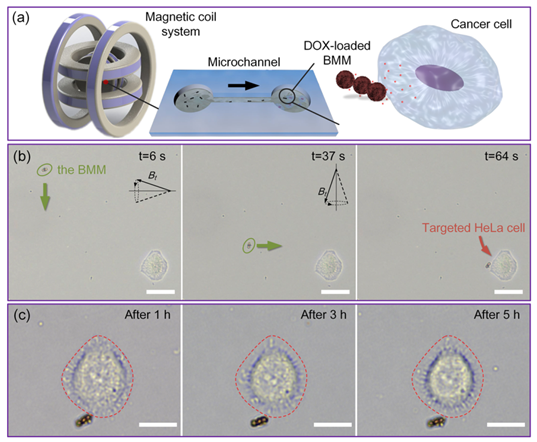
圖4,BMMs的體外靶向給藥試驗。
BMMs具有兩種不同的運動模式,包括動態磁場下的旋轉和垂直旋轉磁場下的翻滾;運動速度的測量以及精確定位的實現表明BMMs具有優異的驅動能力(圖2)。BMMs還表現出良好的生物相容性、高效的DOX裝載能力、pH觸發釋藥能力以及顯著的化療效果(圖3)。另外,采用PμSL(nanoArch S140微納3D打印設備, 摩方精密)技術結合PDMS倒模技術制備了啞鈴形微流控通道,在該通道內,利用磁場驅動實現了BMMs對HeLa癌細胞的靶向給藥。結果表明BMMs可以實現精準靶向給藥,并對抗腫瘤治療具有良好的療效。此研究在靶向抗癌治療方面具有巨大的應用潛力。該研究成果,以“Magnetic Biohybrid Microrobot Multimers Based on Chlorella Cells for Enhanced Targeted Drug Delivery”為題發表在ACS Applied Materials & Interfaces上。
原文鏈接:
https://doi.org/10.1021/acsami.1c16859